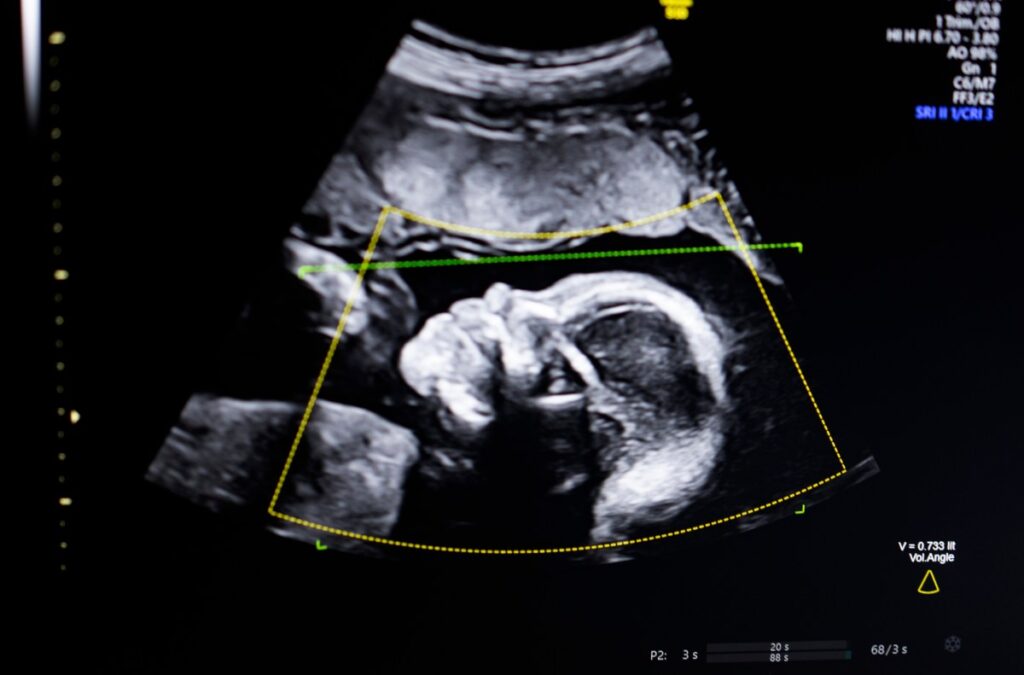
BioticsAI, ganador de TechCrunch Disrupt Battlefield 2023, anunció el lunes que recibió la autorización de la FDA para su software de inteligencia artificial que ayuda a detectar anomalías fetales a partir de imágenes de ultrasonido.
El producto fue concebido por el fundador y director ejecutivo Robbie Bustami, quien creció en una familia de obstetras, incluidos su madre, su tía y su tío. Pasó mucho tiempo en hospitales durante su infancia y, a menudo, viajaba con su madre mientras ella lo cuidaba por todo Estados Unidos.
Después de estudiar codificación y ciencias de la computación en la Universidad de California, Irvine, Bustami lanzó BioticsAI en 2021 en colaboración con Salman Khan, Chaskin Salov y el Dr. Hisham El-Gamal.
La tecnología utiliza IA de visión por computadora para «respaldar la evaluación de la calidad de la ecografía fetal, la integridad anatómica, los informes automatizados y la integración perfecta en los flujos de trabajo clínicos», dijo Bustami a TechCrunch.
Espera que su tecnología ayude a combatir el hecho de que Estados Unidos tiene algunos de los peores resultados prenatales para las madres entre los países de altos ingresos. Las mujeres negras en particular enfrentan tasas de mortalidad materna extremadamente altas;
Bustami dijo que las ecografías prenatales son la «piedra angular» del seguimiento del embarazo, pero la mala calidad de las imágenes puede provocar diagnósticos erróneos.
Bustami dijo que el mayor desafío no era construir un modelo de IA entrenado en un conjunto diverso de cientos de miles de ultrasonidos, sino garantizar que la tecnología funcionara de manera confiable en el mundo real, particularmente en los grupos demográficos con mayor riesgo de sufrir un resultado trágico.
evento de crisis tecnológica
san francisco
|
13-15 de octubre de 2026
«En un entorno donde las disparidades en los resultados de la atención médica están bien documentadas, era importante mostrar un desempeño consistente no sólo en el caso ideal sino en todos los subgrupos de pacientes», continuó Bastami.
El director ejecutivo dijo que tomó poco menos de tres años pasar por el proceso de la FDA, que incluye probar y validar el producto. Esta experiencia le enseñó a él y a su equipo lo importante que es tener operaciones de ingeniería, productos, clínicas y regulatorias estrechamente alineadas desde el principio. «Al diseñar el producto, la validación clínica y la vía regulatoria de forma conjunta en lugar de secuencialmente, pudimos avanzar rápidamente», afirmó.
Ahora que recibió la aprobación de la FDA, Bustami dijo que el próximo objetivo de la compañía es expandirse a varios sistemas de salud en todo el país. También tiene planes de agregar más capacidades para la medicina fetal y la salud reproductiva.
«Estamos bien posicionados para ampliar tanto la distribución como el impacto clínico mientras continuamos profundizando el poder de nuestra tecnología», afirmó.
Este artículo se ha actualizado para corregir la ortografía del nombre del cofundador.
Source link